Vulkanismus Grundlagen
Vulkanische Seen: Blaue Fenster in die Tiefen eines Vulkans
- Von allen bekannten Oberflächengewässern auf der Erde zeigen vulkanische Seen die größte Bandbreite an pH-Werten.
- Kraterseen und kohlendioxid-reiche Seen bedürfen besonders genauer Überwachung hinsichtlich ihrer Gefahren.
- Für die Überwachung von Vulkanen können Farbveränderungen in den vulkanischen Seen sowie das Vorhandensein und die Morphologie von Schwefelkügelchen ein einfaches Hilfsmittel sein.
- Es gibt die Hoffnung, dass einige Bakterien aus vulkanischen Seen das Pflanzenwachstum unter extremem abiotischen Stress fördern können. Unter Umständen sind diese Bakterien von Nutzen für Pflanzen, die anderswo auf sauren, Schwermetall-belasteten Böden gedeihen oder großen Hitzestress aushalten müssen.
Vulkanische Seen mit ihren teils unnatürlich anmutenden Wasserfarben und kontrastreichen mineralischen Ablagerungen faszinieren. Einige von ihnen sind ungewöhnlich tief oder aber ihr Wasser ist extrem sauer und praktisch ohne Leben, in manchen wiederum vermehren sich Cyanobakterien oder Algen zügellos – je nachdem wie eng die Verbindung zwischen dem vulkanischen System und dem Untergrund noch ist. Solche Seen können einen Einblick in hydrothermale Systeme gewähren und somit bei der Überwachung von Vulkanen und der Gefahrenvorhersage von großem Wert sein. Sie können – teils längst verebbte – vulkanische Aktivität bezeugen. Einige von ihnen sind hinsichtlich ihrer Wasserchemie oder -biologie kaum noch von einem herkömmlichen Gewässer zu unterscheiden. Besteht jedoch noch eine Verbindung zu Magmakammern in der Erdkruste, dann sind sie praktisch nie stabile Systeme.
Vulkanische Seen können wieder verschwinden, abfließen, ihre Wassertemperaturen und chemische Zusammensetzung können großen Schwankungen unterliegen und der pH-Wert kann zum Teil deutlich variieren. Grundsätzlich müssen einige Dinge zusammenkommen, damit ein aktiver vulkanischer See entsteht: der Seeboden muss so abgedichtet sein, dass Wasser nicht direkt versickert, der meteorologische Niederschlag muss möglichst reichlich und der Wärmeeintrag nur begrenzt sein, damit das Seewasser nicht völlig verdunstet. Vulkanischen Fluide tragen dann zum Volumen des Sees bei.
Es gibt verschiedene Möglichkeiten vulkanische Seen zu klassifizieren – nach chemischen oder physikalischen Merkmalen oder auch hinsichtlich ihrer Genese. Sie sind in der Monographie „Volcanic Lakes“ (Rouwet et al., 2015) ausführlich zusammengestellt. Wissenschaftler*innen orientieren sich an vier Leitfragen, welche die Entstehung der Seen betreffen. Zum einen ist demnach die Kenntnis essentiell, ob ein See bei einem einzigen Ausbruch entstanden, also z.B. monogenetisch ist. Das hieße, dass unter Umständen seit dem Ereignis der Einfluss des Vulkanismus auf das Seewasser nur noch gering oder gar inexistent ist. Entsteht hingegen ein Seebecken auf einem polygenetischen Vulkan, so können viele verschiedene Ereignisse sowie Magmaquellen zu seiner Entstehung beigetragen haben oder weiterhin beitragen.
Ein weiteres Kriterium beleuchtet den zeitlichen Zusammenhang zwischen Vulkanismus und Herausbildung des Sees, sprich die Frage: entstand der See kurz oder eher lange nach einem Vulkanausbruch? Caldera-Seen sind vermutlich meist lange nach dem Kollaps einer Magmakammer und der daraus entstandenen Senke (geolog.: „Depression“), die dann zum Seebecken wird, entstanden. Seen in Gipfelkratern aktiver Vulkane entstehen hingegen „kurz“ nach einem Vulkanausbruch. Auch kommt es auf den Standort des vulkanischen Sees im Verhältnis zum Vulkanschlot an. Liegt der See unmittelbar über einem aktiven Schlot oder neben diesem? All diese Aspekte bestimmen letztendlich, wie stark sich Vulkanismus, Wasserchemie und Wassertemperatur gegenseitig beeinflussen (Christenson et al., 2015). Dieses generische Klassifizierungssystem hilft, eine Verbindung zu den klassischeren Ansätzen der chemischen und physikalischen Klassifizierungen von Vulkanseen herzustellen.
Nach solchen Klassifikationen umfasst eine Kategorie zum Beispiel Kraterseen, die über dem Schlot eines polygenetischen Vulkans entstehen. Kraterseen befinden sich in der Regel im Innern des Vulkangipfelkraters, können sehr tief oder sehr wertvoll im Wasservolumen sein, was auf Schwankungen der Flüssigkeitskondensation, der Verdunstung an der Oberfläche, der Regenwasserbeiträge von Versickerungen oder Überläufen aus dem See zurückzuführen ist (Varekamp et al., 2015). Eine weitere Kategorie bilden Caldera-Seen, so zum Beispiel der Bolsena-See in Italien, der wie viele Caldera-Seen kaum Zu- oder Abflüsse hat. Man nennt sie in den Geowissenschaften endorheische Becken, da sie keinen Abfluss ins Meer besitzen.
Die allermeisten vulkanischen Seen liegen in Maaren, die auch Maar-Diatreme genannt werden. Maare sind üblicherweise Zeugen eines einzigen phreatomagmatischen Ausbruchs. Was danach übrig bleibt, ist praktisch ein fast perfekt kreisförmiges „Loch“ in der Erde, da eine einzige Eruption nicht in der Lage war, einen großen Vulkankegel zu bilden. Wenn die grundwasserführende Schicht (Aquifer) den Maarkrater schneidet, entsteht ein Maarsee. Diatreme durchbrechen die Erdoberfläche und erzeugen eine steile umgekehrte Kegelform. Manchmal enthalten ihre vergrabenen brekziösen Strukturen Mineralien wie Diamanten. Maarkrater sind typischerweise weniger als zwei Kilometer im Durchmesser. Beispiele für Maare bzw. Maarseen sind der Laacher See, der Ulmener Maar, der Blue Lake in Australien oder auch der Aci Gölü See in der Nähe von Karapınar in der Türkei.
Geothermische Seen befinden sich in einer vulkanisch aktiven Umgebung, in der sich durch phreatische Eruptionen Krater gebildet haben, die im Nachhinein von eher kleinen Seen aufgefüllt wurden. Einige Seen füllen tektonische Senken (Depressionen), die durch Lavafelder oder vulkanische Ablagerungen, die Wasser stauen oder die lokale Hydrologie des Zuflusses oder Abflusses von Wasser beeinflussen, entstanden sind. Acht Prozent der natürlich gestauten Seen weltweit sind auf Vulkanismus zurückzuführen (Costa & Schuster, 1988). Es gibt auch einige Vulkanseen, die entstehen, wenn ein erneut aktiver und damit heißer Vulkanschlot den Schnee im Inneren eines bereits vorhandenen Kraters zum Schmelzen bringt. So geschehen zum Beispiel am Vulkan Chiginagak in Alaska im Jahr 2005.
Es gibt weitere Arten vulkanische Seen einzuteilen, zum Beispiel nach ihrer Wasserchemie oder Wasserbilanz. Wird vor allem auf die vulkanische Aktivität und Gefahr geschaut, dann bietet sich eine Unterteilung in „aktive Kraterseen“, „ruhende Kraterseen“ und „kohlendioxidreiche Seen“ an. Jedwede Klassifizierung ist eine Herausforderung, denn die Vielfalt ist groß und die geologischen Strukturen am Seeboden mancherorts nicht gut bekannt. Die Seen sind zudem häufig hinsichtlich der vulkanischen Aktivität im Untergrund, ihres Umgebungsgesteins und ihren spezifischen klimatischen Bedingungen einzigartig. Daher hat jeder See seine eigenen Merkmale und sollte einzeln betrachtet werden, wenn wir versuchen, mehr in Erfahrung zu bringen und den Geheimnissen, die vulkanische Seen bergen, auf die Spur zu kommen.
Der Crater Lake, ein Caldera-See, liegt auf einer Höhe von 1.883 Metern in Oregon (USA). Gespeist von Regen und Schnee und ohne Abflüsse ist der Kratersee mit 589 Metern der tiefste in den Vereinigten Staaten und der siebentiefste der Welt.
The image was taken by a member of the Expedition 52 crew. Caption by Andi Hollier, Hx5, JETS Contract at NASA-JSC. Nasa Earth Observatory
Rouwet, D., Christenson, B., Tassi, F. & Vandemeulebrouck, J. (Hrsg.). (2015). Volcanic Lakes. Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2
El Chichón, Mexiko (Aufnahme im März 2007)
Der Kratersee El Chichón ist von mittlerer Temperatur (30 °C) und die atmosphärischen Bedingungen sind tropisch, d.h. die Luftfeuchtigkeit und Umgebungstemperatur sind hoch, was wiederum zu einer praktisch unsichtbaren Entgasung und Verdunstung führt.
Foto: Dmitri Rouwet
Kawah Ijen, Indonesien (Aufnahme im September 2014)
Der Kratersee Kawah Ijen ist das größte natürliche, saure Oberflächengewässer der Erde. Das Wasser des Sees ist von einer intensiven türkisen Farbe und weitgehend ohne Leben. Es wurden bisher keine Bakterien oder Eukaryoten gefunden.
Foto: Dmitri Rouwet
Im Ijen-Krater wird auch Schwefel abgebaut, eine schwere und arbeitsintensive Tätigkeit.
Foto: imago images/ZUMA Press
Poás, Costa Rica (April 2007)
Die Laguna Caliente (oben im Bild) ist extrem sauer mit einem pH-Wert von ca -1. Einige saure vulkanische Seen wie auch dieser vulkanische See sind tiefgrau, da die Bodensedimente durch aufsteigende (konvektive) Strömungen aufgewirbelt werden. Der Säuresee ist gesättigt an elementarem Schwefel. In heißen Seen kann sich der flüssige Schwefel am Seeboden ablagern.
Foto: Dmitri Rouwet
Ruapehu Kratersee, Neuseeland (März 2019)
Neben unmittelbaren Gasexplosionen, führt die plötzliche Kondensation der Dampfphase zu einem drastischen Druckabfall, zum Sieden und dann schließlich zu einer hydrothermalen Explosion. Dieser Effekt ist am signifikantesten bei hochaktiven Kraternseen wie z.B. dem Ruapehu in Neuseeland. Lahare entstehen, wenn durch die Explosionen Wasser über den Kraterrand gedrängt wird.
Foto: Dmitri Rouwet
Lake Nyos, Kamerun (Aufnahme im März 2016).
1986 setzte der Nyos-See eine CO2-Wolke in die Atmosphäre frei, die 1.700 Menschen und 3.500 Tiere in den umliegenden Städten und Dörfern tötete. Danach installierten Ingenieure ein Rohrsystem, um das Gas aus dem See abzulassen. Das 200 Meter lange Rohr hängt am Floß und lässt gasreiches Wasser vom Seeboden kontrolliert an die Oberfläche entweichen.
Foto: Dmitri Rouwet
Lake Kivu Ruanda, Demokratische Republik Kongo
Der vulkanische See gehört zu den kohlendioxid-reichen Seen. Die Gefahr durch Gasausbrüche, die sich in der Wassersäule über Jahrzehnte bzw. Jahrhunderte potentiell angesammelt haben, könnte nur durch künstliche und kontrollierte Entgasung der Bodenwasserschicht gebannt werden. Doch für artenreiche Seen wie den Lake Kivu hätte diese Lösung wohl schwerwiegende ökologische Folgen.
Foto: photo MONUSCO / Abel Kavanagh , Lake Kivu (20875703429), CC BY-SA 2.0
Laguna Cuicocha, Ecuador
In der Laguna Cuicocha steigt stetig Kohlendioxid auf. Die vulkanischen Flüssigkeiten haben ihre reaktivsten Komponenten wie Halogene und Schwefel in diesem See weitgehend verloren.
Foto: Sylvain2803, Laguna cuicocha, CC BY-SA 3.0
Was uns Wasserfarben über vulkanische Seen verraten können
Besonders auffällig ist die Vielfalt der Wasserfarben, die vulkanische Seen aufweisen können. Dunkelblau sind häufig solche vulkanischen Seen, die nicht viel Leben bergen, die biologisch unproduktiv sind, weil Nährstoffe fehlen. Ein Beispiel dafür ist der Crater Lake, der im Übrigen ein Caldera-See ist, in Oregon. Mit seiner Tiefe von 589 Metern ist er der tiefste See der USA und siebentiefste der Welt. Der Crater Lake speist sich ausschließlich aus Niederschlägen, hat kaum Zu- oder Abflüsse und erscheint tiefblau.
Grünlich-blau erscheinen Seen, die aus einer wie auch immer gearteten natürlichen oder anthropogenen Quelle Nährstoffe erhalten. Einerseits spielen dafür das Wassereinzugsgebiet und die Düngung der umliegenden landwirtschaftlichen Flächen eine große Rolle. Andererseits können Geothermalquellen mit mineralstoffreichem Wasser ein weiterer Ursprung für Nährstoffe sein. Eine ungewöhnlich starke Grünfärbung kann ein massenhaftes Auftreten von grünen Algen anzeigen, während ein auffälliges Rot mit der starken Vermehrung von Rotalgen zusammenhängt. Zersetzt sich sehr viel organisches Material, dann erscheint ein See in der Regel bräunlich, denn beim Abbau von Blättern und anderem pflanzlichen oder tierischen Material bilden sich organische Säuren.
Grundsätzlich sind die biologischen Prozesse in vulkanischen Seen nicht großartig anders als in Seen nicht-vulkanischen Ursprungs. Doch aufgrund der Chemie in den aktiven Seen können die Farben abweichen: Seen mit Geothermalquellen oder vulkanischen Nährstoffen (aus dem Gestein) enthalten oft Phosphor, der dann zusätzlich düngt. Der Unterschied liegt in diesem Fall eher am ungewöhnlichen Ursprung der Nährstoffe. Andererseits können im Wasser Eisen und Schwefel gelöst sein. Je nachdem, welches Eisen enthalten ist, kann der See dann tiefgrün bei zweiwertigem Eisen (Fe2+) oder violett-bräunlich bzw. orange-rot bei dreiwertigem Eisen (Fe3+) erscheinen. Darüber hinaus können Substanzen, die bestimmte typische Farben aufweisen, ausfällen oder auch im Wasser schweben (z.B. Gipsspat, Schwertmannit, Goethit oder Ferrihydrite). Als der Voui See, der zum Ambae Vulkan (Vanuatu im Südpazifik) gehört, im Jahre 2006 innerhalb weniger Tage blutrot wurde, hat man das später mit dem Ausfällen von Jarosit, einem Sulfat sowie Hämatit, einem Eisenoxid, in Verbindung bringen können (Bani et al., 2009).
Besonders spektakulär sind die türkis-cremeweiß erscheinenden Seen, wie einer der drei Kraterseen des Vulkans Keli Mutu in Indonesien oder auch der größte saure Kratersee der Welt am Kawah Ijen, der ebenso in Indonesien zu finden ist. Die Laguna Caliente am Poás in Costa Rica oder der Yugama Kratersee am Kusatsu-Shirane Vulkan in Japan sind weitere Beispiele. Fein verteilte Schwefelkügelchen (Spherules) schweben hier auf der Wasseroberfläche. Dominieren solche Teilchen völlig, erscheint ein See sehr blau und wird türkis-grünlicher, wenn die Schwefelteilchen abnehmen und sich mit dem Grünton von Eisen-Ionen mischen. Auch siliziumdioxid-reiche geothermische Pools neigen infolge der Streuung des Lichts an winzigen Kolloiden zu einer ganz spezifischen blauen Farbe (Ohsawa et al., 2010). Beobachtungen von Farbveränderungen oder das Vorhandensein und die Morphologie von Schwefelkügelchen können ein einfaches Hilfsmittel zur Überwachung der vulkanischen Aktivität sein. Plötzliche Farbänderungen können zum Beispiel eine Veränderung in der Entgasung von Schwefelgasen widerspiegeln (siehe z. B. Yudamari-See in Japan).
Ein lebensfeindliches Umfeld
Haben wir es mit einem vulkanischen See zu tun, der nicht mit Ausgasungen von Magmakammern in Verbindung steht, dann unterscheidet sich dieser kaum von nicht-vulkanischen Seen – mal abgesehen davon, dass Zu- und Abflüsse fehlen können. Im Englischen spricht man von „neutral dilute volcanic lakes“. Die Wassertemperaturen sind dann ein Spiegel der Wetterverhältnisse und (soweit vorhanden) der Zuflüsse. Der Chemismus des Wassers hängt vom Umgebungsgestein, den Bächen und Flüssen, die ihn durchlaufen bzw. in den See entwässern und der Ausfällung von Mineralen ab.
Wenn Seen noch immer in Verbindung mit entgasenden Magmasystemen stehen, verhält es sich anders. Der Zustand des entgasenden Magmas und die Art des Umgebungsgesteins entscheiden dann ganz immens über die Substanzen im Wasser, Wassertemperaturen und den Säuregrad (pH-Wert). Von allen bekannten Oberflächengewässern auf der Erde zeigen vulkanische Seen die größte Bandbreite an pH-Werten. Der pH-Wert des Seewassers kann außerhalb der Skala liegen, die willkürlich zwischen 0 (sauer) und 14 (alkalisch) festgelegt wurde (Pecoraino et al., 2015). So können die säurehaltigsten Seen, die hochaktive Vulkane bedecken, sogar Wasser mit pH-Werten unter Null aufweisen.
Überblick über die chemische Zusammensetzung des Seewasser von ausgewählten Natronseen. Diese alkalischen Seen kommen besonders häufig in ariden/semi-ariden Klimazonen vor. In ihrem Wasser ist besonders viel Natrium gelöst und der pH-Wert liegt zwischen 8 und 11.
Grafik: Wissensplattform Erde und Umwelt, eskp.de
Zahlen aus: Rouwet et al., 2015
Am anderen Ende der pH-Wert-Skala ermöglichen extrem alkalische Bedingungen eine bemerkenswerte Primärproduktion natronreicher Seen. Bis zu 10 Gramm Kohlenstoff pro Quadratmeter und Tag, d.h. mehr als 15 Mal so viel wie produktive Gewässer und Flüsse (0,6 g C m2 d-1) sind möglich. Vermutlich sind es die produktivsten Gewässer überhaupt, d.h. sie erzeugen die meiste pflanzliche Biomasse pro Quadratmeter. Optimal sind die relativ hohen Umgebungstemperaturen, hohe Lichtintensitäten, die Verfügbarkeit des Nährstoffes Phosphat und der praktisch unbegrenzte Zugang zu CO2 in solchen, an Karbonat reichen Gewässern (Melack & Kilham, 1974; Grant et al., 1990).
Die großen Flamingo-Schwärme in Afrika profitieren davon ganz beträchtlich. Meist ist es sogar nur ein Cyanobakterium Spirulina sp., welches sich in den Natronseen exorbitant vermehrt und deren gesamte Nahrungsgrundlage darstellt. In diesen Seen gibt es zudem eine Reihe alkalitoleranter Bakterien, deren Enzyme zum Teil eine erhebliche wirtschaftliche Bedeutung erlangt haben, u.a. in der Waschmittelindustrie als Bio-Detergenzien.
Seen an hochaktiven Vulkanen können pH-Werte unter Null aufweisen.
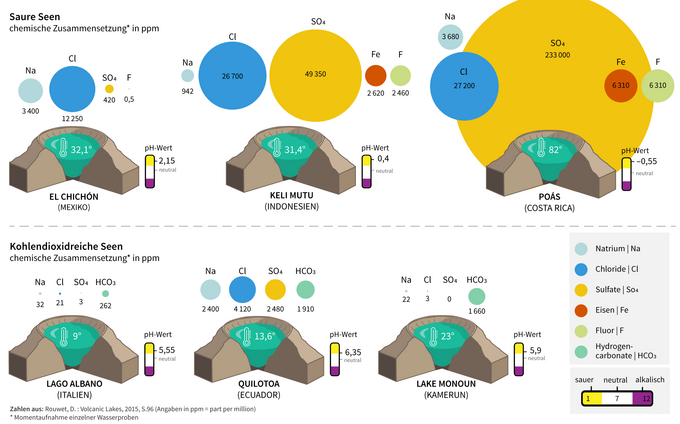
Die chemische Wasserzusammensetzung wird durch vulkanische Fluideinträge und von vulkanischen Gasen beeinflusst. Es kommt dabei zu einer großen Variation von verdünnten Lösungen durch Eintrag von Regen oder Schnee bis zu sehr konzentrierten Säureseen ohne Wasseraustausch. Charakterisiert werden saure vulkanische Seen durch einen niedrigen pH-Wert (bis 6) und die chemischen Hauptelemente CO2, Chloride und Sulfate.
Grafik: Wissensplattform Erde und Umwelt, eskp.de
Das andere Extrem sind vulkanische Seen, die ausgesprochen lebensfeindlich sein können. Oft liegen ihre pH-Werte unter drei. Das ist der Fall, wenn sie eng mit aktivem Vulkanismus und erst kürzlich verebbter vulkanischer Aktivität verknüpft sind.
Sehr saure Seen sind häufig äußerst schwefelreich und haben einen extrem hohen Salzgehalt. Hierfür gibt es zahlreiche Beispiele: die Laguna Caliente am Poás in Costa Rica, der Ruapehu Kratersee in Neuseeland oder auch Kawah Ijen in Indonesien. Allen gemein sind die extrem niedrigen pH-Werte von unter Null bis knapp über 1. Kein höheres Lebewesen kann dieses Wasser trinken, geschweige denn darin leben. Solche pH-Werte entsprächen ungefähr dem unserer Magensäure (nüchtern), welche dafür gemacht ist, Krankheitserreger möglichst unschädlich zu machen.
Es gibt auch Vulkanseen, die hydrothermale Fluide enthalten. Diese hydrothermalen Fluide unterlagen bereits Umwandlungsprozessen und können stark mineralisiert sein. Jedoch tendieren sie dazu, weniger reich an vulkanogenen Komponenten wie Schwefel und Halogenen zu sein. Beispiele für solche Seen finden sich am Taal (zumindest bevor es zum Ausbruch im Januar 2020 kam) sowie am Pinatubo, der wie der Taal-Vulkan zu den Philippinen gehört. Weitere Beispiele sind der Kelut in Indonesien oder auch El Chichón in Mexiko.
Hohe Wassertemperaturen
Wassertemperaturen in nicht-vulkanischen Seen hängen logischerweise stark mit der Lufttemperatur zusammen. Bei vulkanischen Seen ist das nicht unbedingt der Fall. Hier kann die Wassertemperatur stark variieren. Die Wassertemperatur des Ruapehu, dem Kratersee im Gipfel-Krater von Neuseelands höchstem Vulkan (2.797m), beispielsweise schwankt zwischen 10 und 50 °C. Kein höherer Organismus kann mit solchen, teils auch noch plötzlich auftretenden, Temperaturschwankungen umgehen. Sogar kochend heißes Wasser ist möglich: Im See Karymsky in der Caldera Academia Nauk in Kamschatka fing das Wasser während eines Ausbruchs an zu köcheln. Unter diesen schwierigen Bedingungen überleben oft nur Mikroorganismen.
Die Analyse der Mikroorganismen-Gemeinschaft und deren DNA kann auch Aufschluss darüber geben, wie das erste Leben ursprünglich auf der Erde ausgesehen haben könnte. Deshalb wurden zum Beispiel vom Deutschen GeoForschungsZentrum im Rahmen des Interkontinentalen Bohrprogramms (ICDP) am Lake Towuti (Indonesien) sehr tief liegende Sedimente in vulkanischen Seen untersucht, die durch die Bohrkerne zugänglich wurden. Der Lake Towuti kann stellvertretend als modernes Äquivalent zu den eisenreichen Ozeanen im Archaikum, d.h. der Zeit von der Entstehung der Erde bis vor etwa 2,5 Milliarden Jahren, angesehen werden. Die mikrobiellen Gemeinschaften erlauben Rückschlüsse auf das Klima vergangener Zeiten (Paläoklima).
Wissen wir mehr über die Mikroorganismen in vulkanischen Seen, die unter extremsten Bedingungen überleben, ist das ein Wissen, das auch auf andere Kontexten übertragen werden könnte – etwa bei Antworten auf Fragen wie: Welche Organismen sind potentiell in der Lage, völlig degradierte, versauerte Böden zu besiedeln? Welche Organismen könnten zum sogenannten Bio-Mining bzw. Metall-Biolaugung eingesetzt werden, bei der aus Erzen mittels Mikroorganismen Wertmetalle gewonnen werden? Können Bakterien beispielsweise bei der Rückgewinnung toxischer Metalle oder beim Extrahieren begehrter Elemente wie Gold aus dem Gestein eingesetzt werden? Ein Bakterium namens Acidothiobacillus ferrooxidans erwies sich bereits als sehr brauchbar, da es die Mengen an toxischem Chrom und Zink in Klärschlamm auf ein akzeptables Level bringen konnte.
Darüber hinaus gibt es die Hoffnung, dass einige Bakterien aus vulkanischen Seen das Pflanzenwachstum unter extremen abiotischen Stress fördern können, d.h. sie sind nützlich für Pflanzen, die auf degradierten sauren, Schwermetall-belasteten Böden oder bei großem Hitzestress gedeihen müssen. Vor allem bestimmte Bakterien, die Wurzeln von Pflanzen an vulkanischen Seen besiedeln können, haben Mechanismen entwickelt, um diese von giftigen Schwermetallen zu befreien (Mapelli et al., 2015). Am El Chichón-Vulkan in Mexiko hat man bereits ein vielversprechendes Bakterium entdeckt und isolieren können.
Gefahren an vulkanischen Seen
Die Überwachung vulkanischer Seen hilft bei der Einschätzung der potentiellen Gefährdung durch Vulkane. Gleichzeitig gehen von vulkanischen Seen selbst auch Gefahren aus. Auf welche Parameter bei der Überwachung von vulkanischen Seen zu achten ist, erörtert das Interview mit Dr. Egbert Jolie vom Deutschen GeoForschungsZentrum in diesem Themespezial näher (Jolie, 2020). Einige Gefahren, die mit vulkanischen Seen verbunden sind, seien hier kurz umrissen.
Am vulkanischen See des Taal-Vulkans (Philippinen) starben im Jahre 1911 durch Tsunamis und Seichen viele Fischer. Insgesamt ließen in den bis zu 5 m hohen Wellen mehr als 1.300 Menschen ihr Leben. Solche Ereignisse − mit Seichen und Tsunamis − gab es beispielsweise auch am Taupo-See in Neuseeland und am Spirit Lake am Mount St. Helens in den USA.
Seichen sind stehende Wellen, die sich in jedem geschlossenen oder halbgeschlossenen Wasserkörper/-becken bilden können. Die stehenden Wellen sind die Summe zweier Wellen, welche sich in entgegengesetzte Richtungen ausbreiten – bei vulkanischen Seen beispielsweise ausgelöst durch ein Erdbeben, subaquatische Explosionen wie am Lake Managua, schwere Sturmfronten oder ähnliche Ereignisse. Das Wasser (und die Wellen) laufen dann noch Stunden oder sogar Tage hin und her. Die größte Amplitude, also größte Wellenhöhe, der stehenden Wellen, ist an jedem Ende des Wasserkörpers zu finden, während sehr kleine Schwingungen am „Knoten“ oder Mittelpunkt der Welle auszumachen sind. Eine Animation der Wetter- und Ozeanografie-Behörde der Vereinigten Staaten (NOAA) veranschaulicht das Prinzip gut. Bei allen hier genannten Gefahren ist immer zu bedenken, dass nicht zwingend Menschen so nah an einem vulkanischen See leben, um wirklich gefährdet zu sein.
Woher stammen Gase in vulkanischen Seen?
Ein weiteres Gefahrenpotential bergen Ausgasungen und Gasansammlungen in vulkanischen Seen in einigen Regionen der Erde. Im Allgemeinen sind die Gase in vulkanischen Seen entweder magmatischen Ursprungs (Kohlendioxid, Schwefeldioxid, Schwefelwasserstoff, Salz- und Flusssäure, Wasserdampf) oder atmosphärischen Ursprungs (Stickstoff, Sauerstoff, Argon und andere Gase in geringen Mengen). Gase wie Methan, Ammoniak, Schwefelsäure können auch aus hydrothermalen Quellen entweichen und zum Seewasser beitragen. Abgesehen davon entstehen Gase im Stoffwechsel aller in einem See lebenden Organismen.
Hinzu kommt eine „Myriade“ an Gasen in geringeren Konzentrationen (z.B. Methan, Kohlenmonoxid, Helium, Wasserstoff). Die meisten dieser Gase führen vor allem dazu, dass das Seewasser saurer wird.
Ein Beispiel für einen See, der regelmäßig entgast, ist der Albaner See in Italien – insbesondere im Winter wird Kohlendioxid freigesetzt. Der Albaner See liegt nur 25 Kilometer südöstlich von Rom in einem polygenetischen Maar (z.B. Giaccio et al., 2009). Er könnte eine direkte Verbindung zu einer langlebigen Magmakammer haben. Daher ist eine kontinuierliche Überwachung der Physikochemie, der mikrobiellen Aktivität, und der gelösten Gase wie z.B. des Kohlendioxids, unerlässlich. Zu großen Kohlendioxidfreisetzungen kam es allein in der nahen Vergangenheit in den Jahren 1829, 1927 und 1989. Eine rückblickende Analyse der Aktivität lässt vermuten, dass sich CO2 so stark ansammelt, wie das am Lake Nyos und Monoun in Kamerun der Fall ist (Rouwet et al., 2019).
Seen müssen tief genug sein, um Gas unter hohem Druck gelöst zu halten, und auch groß genug, damit sich erhebliche CO2-Mengen im Wasser lösen können. Nur wenn sie stark geschichtet sind und diese Schichtung (Stratifizierung) für mehrere Jahre bis Jahrzehnte aufweisen, ist die Ansammlung von Gasen in den tiefen, kühleren Wasserschichten möglich.
Die meisten Seen in gemäßigtem Klimazonen mischen sich ein- oder zweimal pro Jahr und geben dann zeitgleich ihre gespeicherten Gase in die Atmosphäre ab. Bei meromiktischen Seen hingegen, deren Wasser sich nie völlig durchmischt, kann es über 100 bis 1000 Jahre zur Gasspeicherung kommen. Eine stabile Stratifizierung wie zum Beispiel im Lake Nyos oder Monoun in Kamerun wird durch steile und unter Wasser liegende Kraterwände, die das Wasserbecken formen, ermöglicht. Eine windbedingte Vermischung wird unter diesen Bedingungen verhindert und durch die geringe jahreszeitliche Abkühlung des tropischen Klimas ist die tiefe vertikale Durchmischung begrenzt.
Es muss eine ausdauernde lokale Quelle für Kohlendioxid geben, damit anscheinend ruhende Maar-Seen wie Lake Nyos oder Lake Monoun zu „Killer-Seen“ werden. Die sogenannte Kamerun-Vulkanlinie ist ein weltweiter Hotspot von Seen, die geringe, aber praktisch konstante Mengen an magmatischen Gasen ausstoßen. Die geologische Ursache geht auf die Spaltung Afrikas und Südamerikas und die Öffnung des Atlantischen Ozeans zurück, die vor etwa 120 Millionen Jahren begann. Kohlendioxideinträge in Form von CO2-geladenem Natriumkarbonat-reichen Grundwasser mit niedriger Temperatur sind entlang des Kameruner Vulkangebirges weit verbreitet (Tanyileke et al., 1996). Frei werden können die Gase unter anderem, wenn eine Erschütterung oder anderer äußerer Einfluss zur Vermischung der Wasserschichten führt. Das kann ein Erdbeben, ein vulkanisches Ereignis oder ein Erdrutsch sein.
Zu fatalen Entgasungen kam es sowohl am Nyos-See wie auch am Monoun-See in Kamerun. Der Gasausbruch fand hier wahrscheinlich nur deshalb statt, weil das gelöste CO2 im Tiefenwasser von Nyos und Monoun in Verbindung mit der Periode weniger stabiler Schichtung des Sees in der Regenzeit (Sommer) stand, und Übersättigungswerte erreichte und sich auflöste (Kusakabe, 2015). Am Nyos-See liefen im Jahre 1986 etwa 1,94 × 106 Tonnen CO2 in einer Gaswolke über den Kraterrand und zogen als dichte Strömung über zehn Kilometer entlang eines Flusstals stromabwärts. Das über Land strömende farb- und geruchlose Kohlendioxid hat eine größere Dichte als Luft, schwebte also dicht am Boden und erstickte 1.800 Menschen, die in der Nähe des Sees lebten. Solche Ereignisse sind sehr selten, obwohl CO2-Quellen in vielen vulkanischen Regionen üblich sind. Dennoch sind global kaum Analoga bekannt.
An vulkanischen Seen sind auch gefährliche pyroklastische Ströme möglich. Besonders tragisch war ein solcher Strom am Vulkan Soufrière auf der Karibikinsel St.Vincent im Jahre 1902. Der Kratersee wurde bei der explosiven Eruption herausgeschleudert und die pyroklastischen Ströme waren für einen Großteil der 1.680 Toten verantwortlich. Schlamm- und Schuttströme, sogenannte Lahare, sowie phreatomagmatische Explosionen, die entstehen, wenn Magma in Kontakt mit Wasser kommt, sind weitere Gefahren und decken sich mit Gefahren, die von Vulkanen ausgehen. Der ESKP-Artikel „Umgang mit Naturgewalten – Verhalten an aktiven Vulkanen“ gibt zu diesen Gefahren einen detaillierten Überblick (Zorn, 2020).
Wer mehr über vulkanische Seen in Erfahrung bringen möchte, kann sich mit der Monographie „Volcanic Lakes“ befassen. Die Informationen dieses Artikels basieren auf dieser umfassenden Publikation, welche von Dmitri Rouwet, Bruce Christenson, Franco Tassi und Jean Vandemeulebrouck in Zusammenarbeit mit vielen Wissenschaftskollegen*innen 2015 erarbeitet und herausgegeben wurde. Die Monographie richtet sich vornehmlich an Experten, u.a. Vulkanologen und Biologen und gibt einen umfangreichen und vertiefenden Einblick in die Forschung zu vulkanischen Seen. Sie kann daher vor allem als weiterführende Lektüre empfohlen werden.
Referenzen
- Bani, P., Oppenheimer, C., Varekamp, J. C., Quinou, T., Lardy, M. & Carn, S. (2009). Remarkable geochemical changes and degassing at Voui crater lake, Ambae volcano, Vanuatu. Journal of Volcanology and Geothermal Research, 188(4), 347-357. doi:10.1016/j.jvolgeores.2009.09.018
- Caudron, C., Mauri, G., Williams-Jones, G., Lecocq, T., Kamil Syahbana, D., De Plaen, R., Peiffer, L., Bernard, A. & Saracco, G. (2016). New insights into the Kawah Ijen hydrothermal system from geophysical data. In T. Ohba, B. Capaccioni & C. Caudron (Hrsg.), Geochemistry and Geophysics of Active Volcanic Lakes (Special Publications, 437, S. 57-72). London: Geological Society. doi:10.1144/SP437.4
- Christenson, B., Németh, K. Rouwet, D., Tassi, F, Vandemeulebrouck, J. &, Varekamp, J. C. (2015). Volcanic Lakes. In D. Rouwet, B. Christenson, F. Tassi & J. Vandemeulebrouck (Hrsg.), Volcanic Lakes (S. 1-20). Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2_1
- Costa J. E. & Schuster R. L. (1988). The formation and failure of natural dams. GSA Bulletin, 100(7), 1054-1068. doi:10.1130/0016-7606(1988)100<1054:TFAFON>2.3.CO;2
- Giaccio, B., Messina, P., Sposato, A., Voltaggio, M., Zanchetta, G., Galadini, F., Gori, S. & Santacroce, R. (2009). Tephra layers from Holocene lake sediments of the Sulmona Basin, central Italy: implications for volcanic activity in Peninsular Italy and tephrostratigraphy in the central Mediterranean area. Quaternary Science Reviews, 28(25-26), 2710–2733. doi:10.1016/j.quascirev.2009.06.009
- Grant, W. D., Mwatha, W. E. & Jones, B. E. (1990). Alkaliphiles: ecology, diversity, and applications. FEMS Microbiology Reviews, 6(2-3), 255-269. doi:10.1111/j.1574-6968.1990.tb04099.x
- IAVCEI Commission on Volcanic Lakes. (o.D.). [iavcei-cvl.org, Blog]. Aufgerufen am 26.06.2020.
- Jolie, E. (2020). Konzepte für die Überwachung vulkanischer Seen. In D. Spreen, J. Kandarr, P. Klinghammer & O. Jorzik (Hrsg.), ESKP-Themenspezial Vulkanismus und Gesellschaft. Zwischen Risiko, Vorsorge und Faszination (S. 166-169). Potsdam: Helmholtz-Zentrum Potsdam, Deutsches GeoForschungsZentrum GFZ. doi:10.2312/eskp.2020.2.7.6
- Kusakabe, M. (2015). Evolution of CO2 content in Lakes Nyos and Monoun, and sub-lacustrine CO2-recharge system at Lake Nyos as envisaged from C/3He ratios and noble gas signatures. In D. Rouwet, B. Christenson, F. Tassi & J. Vandemeulebrouck (Hrsg.), Volcanic Lakes (S. 427-450). Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2_19
- Mapelli, F., Marasco, R., Rolli, E., Daffonchio, D., Donachie, S. & Borin, S. (2015). Microbial Life in Volcanic Lakes. In D. Rouwet, B. Christenson, F. Tassi & J. Vandemeulebrouck (Hrsg.), Volcanic Lakes (S. 507-522). Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2_23
- Melack, J. M. & Kilham, P. (1974). Photosynthetic rates of phytoplankton in East African alkaline, saline lakes. Limnology and Oceanography, 19(5), 743-755. doi:10.4319/lo.1974.19.5.0743
- National Oceanic and Atmospheric Administration – NOAA. (2018, 25. Juni). What is a seiche? [National Ocean Service website, oceanservice.noaa.gov]. Aufgerufen am 26.06.2020.
- Ohsawa, S., Saito, T., Yoshikawa, S., Mawatari, H., Yamada, M., Amita, K., Takamatsu, N., Sudo, Y. & Kagiyama, T. (2010). Color change of lake water at the active crater lake of Aso volcano, Yudamari, Japan: is it in response to change in water quality induced by volcanic activity? Limnology, 11(3), 207-215. doi:10.1007/s10201-009-0304-6
- Pecoraino, G., D’Alessandro, W. & Inguaggiato, S. (2015). The Other Side of the Coin: Geochemistry of Alkaline Lakes in Volcanic Areas. In D. Rouwet, B. Christenson, F. Tassi & J. Vandemeulebrouck (Hrsg.), Volcanic Lakes (S. 219-237). Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2_9
- Rouwet, D., Christenson, B., Tassi, F. & Vandemeulebrouck, J. (Hrsg.). (2015). Volcanic Lakes. Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2
- Rouwet, D., Giovanni Chiodini, G., Ciuccarelli, C., Comastri, A. & Costa, A. (2019). Lago Albano, the “anti-Nyos-type” lake: The past as a key for the future. Journal of African Earth Sciences, 150, 425-440. doi:10.1016/j.jafrearsci.2018.09.019
- Tanyileke, G. Z., Kusakabe, M. & Evans, W. C. (1996). Chemical and isotopic characteristics of fluids along the Cameroon volcanic line, Cameroon. Journal of African Earth Sciences, 22(4), 433-441. doi:10.1016/0899-5362(96)00025-5
- Varekamp, J. C. (2015). The Chemical Composition and Evolution of Volcanic Lakes. In B. Christensen, K. Németh, D. Rouwet, F. Tassi, J. Vandemeulebeck & J.-C. Varekamp (Hrsg.), Volcanic Lakes (S. 93-123). Berlin/Heidelberg: Springer. doi:10.1007/978-3-642-36833-2_4
- Zorn, E. (2020). Umgang mit Naturgewalten – Verhalten an aktiven Vulkanen. In D. Spreen, J. Kandarr, P. Klinghammer & O. Jorzik (Hrsg.), ESKP-Themenspezial Vulkanismus und Gesellschaft. Zwischen Risiko, Vorsorge und Faszination (S. 40-44). Potsdam: Helmholtz-Zentrum Potsdam, Deutsches GeoForschungsZentrum GFZ. doi:10.2312/eskp.2020.2.1.5
DOI
https://doi.org/10.2312/eskp.2020.2.1.3
Zitiervorschlag: Kandarr, J. (2020). Vulkanische Seen: Blaue Fenster in die Tiefen eines Vulkans. In O. Jorzik, J. Kandarr, P. Klinghammer & D. Spreen (Hrsg.), ESKP-Themenspezial Vulkanismus und Gesellschaft. Zwischen Risiko, Vorsorge und Faszination (S. 17-25). Potsdam: Helmholtz-Zentrum Potsdam, Deutsches GeoForschungsZentrum GFZ. doi:10.2312/eskp.2020.2.1.3